Neue PRAME-spezifische Immuntherapie IMA203 beim metastasierten Melanom (schwarzer Hautkrebs)

IMA203 – PRAME-spezifische TCR-T-Zellen als neue Immuntherapie beim metastasierten schwarzen Hautkrebs (Melanom)
Dank der Einführung moderner Immuntherapien wie Checkpoint-Inhibitoren hat sich die Prognose für viele PatientInnen mit metastasiertem malignem Melanom in den letzten Jahren deutlich verbessert. Immer mehr Betroffene können eine langfristige Krankheitskontrolle oder sogar ein vollständiges Ansprechen erreichen. Dennoch kommt es bei einem Teil der PatientInnen zu Rückfällen – und für sie braucht es neue, wirksame Therapieoptionen.
Ein vielversprechender Ansatz ist die sogenannte TCR-T-Zelltherapie, die gezielt gegen Tumorzellen vorgeht, die bestimmte Tumorantigene wie PRAME (Preferentially Expressed Antigen in Melanoma) auf ihrer Oberfläche präsentieren. Eine neue Studie zeigt: Diese individualisierte Zelltherapie könnte eine wichtige Rolle in der Behandlung fortgeschrittener Melanome und anderer PRAME-positiver Tumoren spielen.
Was ist PRAME?
PRAME steht für “Preferentially Expressed Antigen in Melanoma”. Es handelt sich dabei um ein Eiweiß, das fast ausschließlich von Krebszellen gebildet wird – bei gesunden Zellen kommt es kaum vor.
Das macht PRAME zu einem idealen Ziel für neue Therapien: Wenn das Immunsystem gezielt auf PRAME-positive Zellen trainiert wird, können die Tumorzellen angegriffen werden – gesunde Zellen bleiben weitgehend verschont.
Bei welchen Krebsarten ist PRAME besonders häufig zu finden?
- Malignes Melanom
- Lungenkrebs
- Eierstockkrebs
- Kopf-Hals-Tumoren
- Sarkome
Wie funktioniert die TCR-T-Zelltherapie gegen PRAME?
Die TCR-T-Zelltherapie ist eine moderne Form der personalisierten Immuntherapie. Sie nutzt körpereigene T-Zellen – also die “Killerzellen” des Immunsystems – sie werden im Labor gezielt verändert, sodass sie gegen Tumorzellen, die das PRAME-Antigen tragen, vorgehen können.
So funktioniert’s Schritt für Schritt:
- T-Zellen entnehmen (Leukapherese): Den Patientinnen und Patienten wird Blut entnommen, um T-Zellen zu isolieren.
- Genetische Umprogrammierung: Im Labor wird den T-Zellen ein künstlicher Rezeptor eingebaut – ein sogenannter T-Zell-Rezeptor (TCR), der ganz speziell auf das PRAME-Antigen reagiert. Nur Tumorzellen mit PRAME werden dadurch erkannt.
- Vermehrung der T-Zellen: Die modifizierten T-Zellen werden in großer Zahl vervielfältigt.
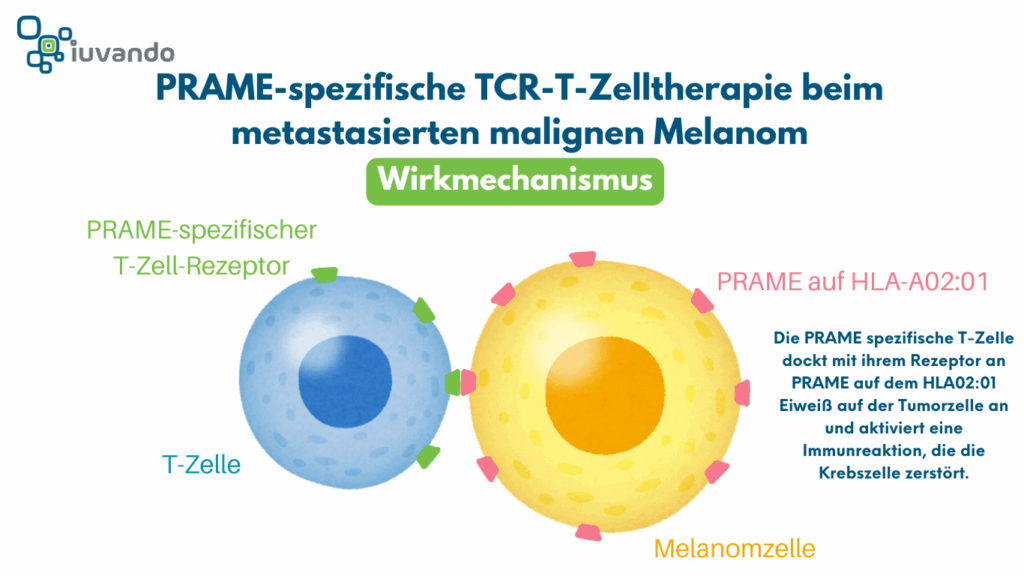
- Rückgabe an den Körper: Die “trainierten” T-Zellen werden dem Patienten zurückgegeben – sie zirkulieren im Blut, erkennen PRAME auf Krebszellen und zerstören diese gezielt.
Der große Vorteil: Im Gegensatz zu herkömmlicher Chemotherapie greift diese Methode nur Krebszellen an, die PRAME tragen, und schont gesunde Zellen. Dadurch kann sie sehr präzise und gleichzeitig wirksam sein – besonders bei schwer behandelbaren Tumoren wie dem metastasierten malignen Melanom.
Allerdings kann IMA203 PRAME nur dann identifizieren, wenn es von einem bestimmten Molekül namens HLA-A02:01 präsentiert wird. Dieses Molekül funktioniert wie eine „Halterung“, die das Peptid sichtbar macht. Da nicht alle Menschen diesen HLA-Typ haben, kann die Therapie nur bei Patientinnen und Patienten mit HLA-A02:01 wirken – bei anderen fehlt die notwendige Präsentation für eine gezielte Immunreaktion.
IMA203 Studie: Studienhintergrund und Zielgruppe
Die in Nature Medicine publizierte Studie untersuchte die Sicherheit und Wirksamkeit einer neu entwickelten T-Zelltherapie namens IMA203 bei Patientinnen und Patienten mit fortgeschrittenen soliden Tumoren. Insgesamt konnten 40 Personen teilnehmen, die zuvor mehrere Therapielinien erhalten hatten und bei denen die Erkrankung weiter fortgeschritten war. Die Tumoren mussten ein bestimmtes Zielmerkmal aufweisen: das PRAME-Protein (Preferentially Expressed Antigen in Melanoma), das in vielen Krebsarten – darunter Haut-, Eierstock-, Gebärmutter-, Lungen- und Kopf-Hals-Tumoren – übermäßig gebildet wird.
Obwohl der Fokus der Publikation auf dem metastasierten malignen Melanom lag (16 der 40 Behandelten), zeigt die Studie, dass diese Form der personalisierten T-Zelltherapie prinzipiell auch bei anderen PRAME-positiven soliden Tumoren wirksam sein könnte.
Wirksamkeit der autologen TCR-T-Zelltherapie IMA203 beim metastasierten malignen Melanom
In der im Fachjournal Nature Medicine veröffentlichten Studie wurden 16 Patientinnen und Patienten mit metastasiertem malignem Melanom mit der autologen TCR-T-Zelltherapie IMA203 behandelt. Alle PatientInnen hatten Tumore, die das Zielantigen PRAME exprimierten.
Gesamte Patientengruppe (n = 16):
-
Eine Tumorverkleinerung (u/cORR) wurde bei 75 % der Patientinnen und Patienten beobachtet.
-
Die Zeit ohne Voranschreiten der Erkrankung betrug 3,3 Monate.
-
Das Gesamtüberleben (OS) lag im Mittel bei 8,1 Monaten.
Patientinnen und Patienten, die höhere Zell-Dosen (DL4/5) erhielten (n = 10):
-
In dieser Gruppe sprachen 70 % der Behandelten auf die Therapie an (u/cORR).
-
Das mittlere Zeit ohne Voranschreiten der Erkrankung lag bei 5,1 Monaten. Das mittlere Gesamtüberleben war zum Zeitpunkt der Auswertung noch nicht erreicht.
Diese Daten zeigen, dass die Therapie auch bei Patientinnen und Patienten mit fortgeschrittenem malignem Melanom – einer Erkrankung, die häufig schwer zu behandeln ist – eine relevante Krankheitskontrolle bewirken kann. Besonders bei höherer Dosierung zeigten sich langanhaltende Ansprechen bei einem Teil der Patientinnen und Patienten.
Was bedeuten uORR, cORR, PFS und OS?
-
uORR (unkorrigierte objektive Ansprechrate): Anteil der Patientinnen und Patienten, bei denen sich der Tumor nach der Behandlung messbar verkleinert hat – unabhängig davon, ob dieses Ansprechen später erneut bestätigt wurde.
-
cORR (confirmed objective response rate): Anteil der Patientinnen und Patienten mit einer nachweislich bestätigten und anhaltenden Tumorverkleinerung – also eine besonders verlässliche Messung des Therapieansprechens.
-
PFS (progressionsfreies Überleben): Zeitraum, in dem die Erkrankung nach Beginn der Therapie nicht weiter voranschreitet. Ein längeres PFS spricht für eine wirksame Krankheitskontrolle.
-
OS (Gesamtüberleben): Zeitraum vom Beginn der Therapie bis zum Tod – unabhängig von der Todesursache. Das OS ist einer der wichtigsten Faktoren zur Bewertung einer Krebstherapie.
Nebenwirkungen und Verträglichkeit der IMA203-Therapie
In der Studie zeigte sich, dass die Nebenwirkungen der autologen TCR-T-Zelltherapie IMA203 insgesamt gut kontrollierbar waren:
-
Zytokinfreisetzungssyndrom (CRS): Diese Immunreaktion trat bei 75 % der Behandelten auf, war jedoch ausschließlich mild (Grad 1–2) und gut behandelbar.
-
ICANS (neurotoxische Effekte): Es wurden keine schwerwiegenden neurologischen Nebenwirkungen wie Verwirrtheit, Sprachstörungen oder Krampfanfälle dokumentiert.
-
Lymphopenie: Eine vorübergehende Abnahme bestimmter weißer Blutzellen wurde häufig beobachtet, normalisierte sich aber in der Regel von alleine.
Kann die TCR-T-Zelltherapie mit IMA203 zur neuen Standardbehandlung nach Versagen der Checkpoint-Therapie beim malignen Melanom werden?
Diese Frage soll die aktuell laufende SUPRAME-Studie (NCT06743126) beantworten.
Die klinische Phase-3 Studie untersucht den Einsatz der autologen TCR-T-Zelltherapie IMA203 bei PatientInnen mit fortgeschrittenem malignen Melanom, die zuvor nicht auf eine Immun-Checkpoint-Blockade angesprochen haben oder danach einen Rückfall erlitten. Im Fokus steht dabei, ob sich durch die gezielte Immuntherapie das Tumorwachstum wirksamer aufhalten lässt als mit bisherigen Therapien.
Was macht die Immuntherapie Studie besonders?
IMA203 ist eine personalisierte Zelltherapie, die T-Zellen der PatientInnen gentechnologisch so verändert, dass sie ein bestimmtes Tumorantigen (PRAME) gezielt erkennen und angreifen können. Anders als klassische Immuntherapien wirkt IMA203 auch unabhängig von PD-1/PD-L1 oder CTLA-4 – also genau den Signalwegen, auf die Checkpoint-Inhibitoren abzielen.
Die SUPRAME-Studie vergleicht IMA203 direkt mit der Standardbehandlung, die ÄrztInnen nach dem individuellen Zustand der PatientInnen auswählen (sogenannter „investigator’s choice“). Dazu zählen z.B. Chemotherapie oder eine erneute Checkpoint-Inhibitor-Behandlung.
Zielgruppe und Studiendesign der SUPRAME Studie beim malignen Melanom
Eingeschlossen werden Erwachsene mit fortgeschrittenem, inoperablem oder metastasiertem malignem Melanom. Alle Teilnehmenden müssen zuvor mit einer PD-1-basierten Immuntherapie, einer sogenannten Checkpoint-Blockade, behandelt worden sein, die entweder keine ausreichende Wirkung zeigte oder nach der es zum Rückfall kam.
Die Studie prüft in zwei Behandlungsarmen:
-
Arm A: IMA203 (einmalige Zellinfusion nach vorbereitender Chemotherapie)
-
Arm B: „Standard of care“, individuell ausgewählt durch das Behandlungsteam
Es wird untersucht ob sich die Zeit ohne eine Voranschreiten der Erkrankung, unterscheidet.
Was erhofft man sich?
Sollte sich IMA203 gegenüber bisherigen Therapien als überlegen erweisen, könnte die PRAME-spezifische TCR-T-Zelltherapie langfristig zu einer neuen Behandlungsoption werden – insbesondere für jene PatientInnen, bei denen alle etablierten Immuntherapien versagt haben.
Die passende Studie zu Ihrer Krebserkrankung
Möchten Sie wissen, ob eine klinische Studie für Ihre individuelle Situation in Frage kommt? Schreiben Sie uns über das Kontaktformular. Wir finden die passende Studie für Sie – kostenlos und unabhängig.
Über den iuvando Patientenblog
Wir brennen für Wissenschaft und wollen Ihnen komplizierte Themen rund um die Krebsforschung einfach verständlich machen, die neuesten Informationen zu Behandlungsmöglichkeiten teilen und mit Ihnen nützliche Tipps für das Leben mit Krebs austauschen.
Wir freuen uns, wenn Sie uns hier oder auf unseren Social Media Kanälen Facebook und instagram begleiten.