Multiples Myelom: Die CAR-T-Zelltherapie mit Cilta-Cel im Fokus

Neue Perspektiven in der CAR-T-Zell-Therapie beim Multiplen Myelom: Die CARTITUDE-4 -Studie mit Cilta-Cel beleuchtet sowohl die Chancen als auch die Risiken dieser innovativen Behandlung.
Wie funktioniert eine CAR-T-Zell-Therapie?
Die CAR-T-Zell-Therapie ist eine personalisierte Form der Immuntherapie. Sie nutzt die körpereigenen Abwehrzellen – sogenannte T-Zellen –, um gezielt Krebszellen anzugreifen.
Der Ablauf:
- Entnahme: T-Zellen werden dem Patienten über das Blut entnommen.
- Modifikation: Diese Zellen werden im Labor genetisch verändert, sodass sie ein spezielles Protein (CAR = Chimeric Antigen Receptor) tragen. Dieses Protein erkennt das Zielmolekül BCMA, das auf den Myelomzellen vorkommt.
- Vermehrung: Die modifizierten T-Zellen werden im Labor vermehrt.
- Rückgabe: Nach einer Vorbereitungstherapie werden die Zellen dem Patienten zurückgegeben, wo sie die Krebszellen erkennen und zerstören sollen.
Dieser innovative Ansatz ist besonders wirkungsvoll, da die T-Zellen gezielt gegen die Zellen des Multiplen Myeloms vorgehen können.
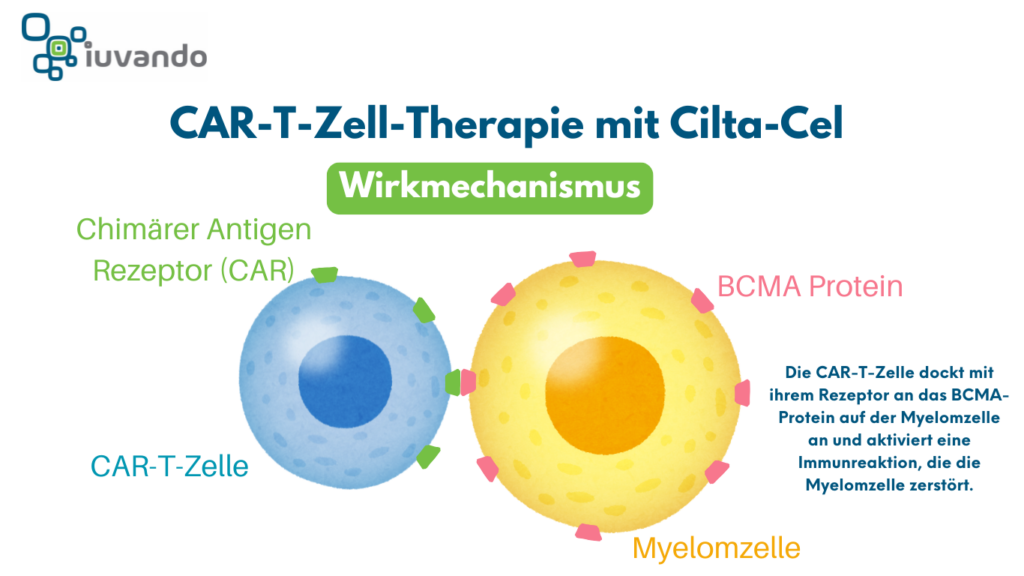
Cilta-Cel als CAR-T-Zell-Therapie beim Multiplen Myelom
Cilta-Cel ist ein speziell entwickeltes CAR-T-Zell-Produkt für PatientInnen mit Multiplem Myelom, bei denen herkömmliche Therapien nicht mehr wirken. Es richtet sich an PatientInnen mit mindestens einer früheren Behandlung, deren Krankheit jedoch weiter voranschreitet. Wichtig: Die Therapie darf nur in spezialisierten Kliniken durchgeführt werden.
Studienergebnisse: Cilta-Cel verlängert das Überleben und verbessert die Lebensqualität beim Lenalidomid-refraktären Multiplen Myelom
Die Wirksamkeit von Cilta-Cel wurde in der internationalen Phase-3-Studie CARTITUDE-4 untersucht, an der 419 PatientInnen mit rezidiviertem oder refraktärem Multiplen Myelom teilnahmen, die zuvor nicht mehr auf eine Behandlung mit Lenalidomid angesprochen hatten.
Höhere Ansprechrate und tiefere Remissionen: Nach einer medianen Nachbeobachtungszeit von 33,6 Monaten erreichten 84,6 % der mit Cilta-Cel behandelten PatientInnen ein objektives Ansprechen, darunter 73,1 % mit einem kompletten Ansprechen (sCR). Im Vergleich dazu lag die Ansprechrate in der Standardtherapiegruppe deutlich niedriger. Zudem wurde bei 61 % der Patient:innen in der Cilta-Cel-Gruppe eine MRD-Negativität (minimale Resterkrankung Negativität) erreicht, verglichen mit 15,6 % in der Standardtherapiegruppe.
Verbessertes Zeit ohne Voranschreiten des Multiplen Myeloms (PFS): Das mittlere PFS wurde in der Cilta-Cel-Gruppe noch nicht erreicht, während es in der Standardtherapiegruppe bei 12,5 Monaten lag. Nach 30 Monaten waren 59,4 % mit Cilta-Cel ohne Anzeichen für einen Voranschreiten oder ein Rezidiv der Erkrankung gegenüber 25,7 % mit der Standardtherapie, was einer Risikoreduktion für Krankheitsprogression oder Tod um 71 % entspricht.
Deutliche Verlängerung des Gesamtüberlebens (OS): Nach 30 Monaten lebten noch 76,4 % der PatientInnen in der Cilta-Cel-Gruppe im Vergleich zu 63,8 % in der Standardtherapiegruppe. Dies entspricht einer Risikoreduktion für den Tod um 45 %. Cilta-cel ist somit die erste CAR-T-Zell Therapie die einen deutlichen Überlebensvorteil bei PatientInnen mit Multiplen Myelom nachweist.
Verbesserte Lebensqualität: PatientInnen, die mit Cilta-Cel behandelt wurden, berichteten über eine deutliche Verbesserungen in der gesundheitsbezogenen Lebensqualität (HRQoL) im Vergleich zur Standardtherapie. Dies umfasste Verbesserungen im Alltag, sowie eine Reduktion von Symptomen wie Schmerzen und Müdigkeit. Die Zeit bis zur Verschlechterung der Symptome wurde mit Cilta-Cel auf median 23,7 Monate verlängert, verglichen mit 18,9 Monaten in der Standardtherapiegruppe.
Nebenwirkungen der CAR-T-Zell Therapie mit Cilta-Cel: Eine starke Therapie mit Risiken
Trotz der vielversprechenden Ergebnisse ist die Behandlung nicht ohne Risiken:
- Starke Immunreaktionen: Bei rund 80 % der PatientInnen kommt es zu einem sogenannten Zytokinfreisetzungssyndrom (CRS). Dies äußert sich durch Fieber, Schüttelfrost und Entzündungen und kann in schweren Fällen lebensbedrohlich werden.
- Neurologische Nebenwirkungen: Etwa 20 % der Betroffenen entwickeln vorübergehende Probleme wie Verwirrtheit, Sprachschwierigkeiten oder Kopfschmerzen.
- Schwere Infektionen: Viele PatientInnen entwickeln Infektionen, die durch ein geschwächtes Immunsystem begünstigt werden. Hierzu zählen auch seltene Erreger, gegen die der Körper normalerweise geschützt ist. Um dies zu verhindern, kann eine Behandlung mit speziellen Antikörpern (Immunglobulinen) sinnvoll sein. Diese Therapie stärkt das Immunsystem, wenn bestimmte Abwehrstoffe (z. B. Immunglobulin G) im Blut fehlen.
- Langfristige Überwachung: Da die Therapie das Immunsystem stark beeinflusst, müssen die PatientInnen lebenslang auf mögliche Spätfolgen, wie die Entstehung weiterer Krebserkrankungen, kontrolliert werden.
Diese Risiken erfordern eine Behandlung an spezialisierten Kliniken mit erfahrenem Personal, das auf solche Komplikationen vorbereitet ist.
Was bedeuten diese Ergebnisse für Patient:innen?
Beide Studien zeigen, dass die Behandlung mit Cilta-Cel beim Multiplen Myelom sehr effektiv ist, aber auch Risiken birgt und daher nur an spezialisierten Zentren durchgeführt werden kann. Dieser Fortschritt in der Behandlung des Multiplen Myeloms spiegelt sich auch in den aktuellen deutschen Leitlinien und internationalen Leitlinien wider, in die CAR-T-Zell Therapie mittlerweile als Standard verankert ist.
Kann die CAR-T-Zell Therapie mit Cilta-cel die autologe Stammzelltransplantation bei PatientInnen mit neu diagnostiziertem Multiplen Myelom ersetzen?
Diese Frage soll die CARTITUDE-6 Studie beantworten:
In dieser Studie können PatientInnen mit neu diagnostiziertem Multiplem Myelom behandelt werden, die bisher keine systemische Therapie erhalten haben.
Ziel der CARTITUDE-6 Studie
In der Studie wird geprüft, ob eine Induktionstherapie gefolgt von einer CAR T-Zell Therapie mit Ciltacabtagene Autoleucel mit anschließender Erhaltungstherapie dem bisherigen Standard einer Induktionstherapie gefolgt von einer Hochdosischemotherapie mit autologer Stammzelltransplantation und Erhaltung überlegen ist.
Ob eine Heilung des Multiplen Myeloms mit einem Standardrisiko durch eine CAR-T-Zelltherapie möglich ist untersucht die aMMbition Studie
In dieser Studie können PatientInnen mit neu diagnostiziertem Multiplem Myelom behandelt werden, die bisher keine systemische Therapie erhalten haben. Es muss ein Standardrisiko bestehen. Link zur Risikoeinschätzung und Prognose beim Multiplen Myelom
Ziel der Studie
Ziel dieser Studie ist es, die Ansprechrate und Anzeichen für eine mögliche Heilung 5 Jahre nach Beginn der Induktionstherapie zu bewerten. Dies ist definiert als eine Kombination aus anhaltender (mindestens 2 Jahre bestehender) Negativität der minimalen Resterkrankung (MRD) mit vollständigem Ansprechen/stringiertem vollständigen Ansprechen und einer Positronen-Emissions-Tomographie/Computertomographie (PET/CT), die nach 5 Jahren keine Anzeichen des Multiplen Myeloms zeigt.
In der Studie gibt es zwei Kohorten:
Kohorte A: Die PatientInnen erhalten eine Induktion mit Dara-VRd + eine Konsolidierung mit Talquetamab (als bispezifischer Antikörper) mit Daratumumab und im Anschluss eine CAR T-Zelltherapie mit Ciltacabtagene Autoleucel.
Kohorte B: In dieser Kohorte erhalten alle PatientInnen eine Induktion mit Dara-VRd, hiernach erfolgt die CAR T-Zelltherapie mit Ciltacabtagene Autoleucel. Im Anschluss erhalten die PatientInnen eine Konsolidierungstherapie mit Talquetamab-Daratumumab und Teclistamab-Daratumumab.
Die passende Studie zu Ihrer Krebserkrankung
Möchten Sie wissen, ob eine klinische Studie für Ihre individuelle Situation in Frage kommt? Schreiben Sie uns über das Kontaktformular. Wir finden die passende Studie für Sie – kostenlos und unabhängig.
Informieren Sie sich bereits jetzt über aktuelle Therapie-Studien beim Multiplen Myelom
Über den iuvando Patientenblog
Wir brennen für Wissenschaft und wollen Ihnen komplizierte Themen rund um die Krebsforschung einfach verständlich machen, die neuesten Informationen zu Behandlungsmöglichkeiten teilen und mit Ihnen nützliche Tipps für das Leben mit Krebs austauschen.
Wir freuen uns, wenn Sie uns hier oder auf unseren Social Media Kanälen Facebook und instagram begleiten.
Quellen:
Mateos M-V, San-Miguel J, Dhakal, et al. Overall Survival (OS) With Ciltacabtagene Autoleucel (Cilta-cel) Versus Standard of Care (SoC) in Lenalidomide (Len)-Refractory Multiple Myeloma (MM): Phase 3 CARTITUDE-4 Study Update. Presented at: 2024 International Myeloma Society Annual Meeting; September 25-28, 2024; Rio de Janeiro, Brazil. Abstract OA – 65.
San-Miguel J et al. Cilta-cel or Standard Care in Lenalidomide-Refractory Multiple Myeloma. New England Journal of Medicine, Veröffentlichung am 5. Juni 2023, N Engl J Med 2023;389:335-347. Link zum Originalartikel
Berdeja, Jesus G et al. Ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study The Lancet, Volume 398, Issue 10297, 314 – 324. Link zum Originalartikel
Lin, Yi et al. Consensus guidelines and recommendations for the management and response assessment of chimeric antigen receptor T-cell therapy in clinical practice for relapsed and refractory multiple myeloma: a report from the International Myeloma Working Group Immunotherapy Committee The Lancet Oncology, Volume 25, Issue 8, e374 – e387. Link zum Originalartikel
Kortüm, Martin et al. Onkopedia Leitlinien Multiples Myelom, Oktober 2024. Link zu Onkopedia
Studienvignette CARTITUDE-6 Studie Link
Studienvignette aMMbition Studie Link