CAR-T-Zelltherapie beim Multiplen Myelom: Häufig gestellte Fragen (FAQ)

Die rasche Entwicklung neuer Therapiemöglichkeiten beim Multiplen Myelom führt zu vielen Fragen von PatientInnen und Angehörigen: In diesem Artikel geben wir fundierte Antworten zur CAR-T-Zelltherapie beim Multiplen Myelom.
Was ist eine CAR-T-Zell-Therapie?
Die CAR-T-Zell-Therapie ist eine personalisierte Immuntherapie, bei der körpereigene T-Zellen gentechnisch verändert werden, um Myelomzellen gezielt zu erkennen und zu zerstören. Die T-Zellen werden aus dem Blut entnommen, im Labor modifiziert und dann als verstärkte Immunzellen zurückgegeben.
Wie funktioniert eine CAR-T-Zell-Therapie?
Die CAR-T-Zell-Therapie ist eine personalisierte Form der Immuntherapie. Sie nutzt die körpereigenen Abwehrzellen – sogenannte T-Zellen –, um gezielt Krebszellen anzugreifen.
Der Ablauf:
- Entnahme: T-Zellen werden dem Patienten über das Blut entnommen.
- Modifikation: Diese Zellen werden im Labor genetisch verändert, sodass sie ein spezielles Protein (CAR = Chimeric Antigen Receptor) tragen. Dieses Protein erkennt das Zielmolekül BCMA, das auf den Myelomzellen vorkommt.
- Vermehrung: Die modifizierten T-Zellen werden im Labor vermehrt.
- Rückgabe: Nach einer Vorbereitungstherapie werden die Zellen dem Patienten zurückgegeben, wo sie die Krebszellen erkennen und zerstören sollen.
Dieser innovative Ansatz ist besonders wirkungsvoll, da die T-Zellen gezielt gegen die Zellen des Multiplen Myeloms vorgehen können.
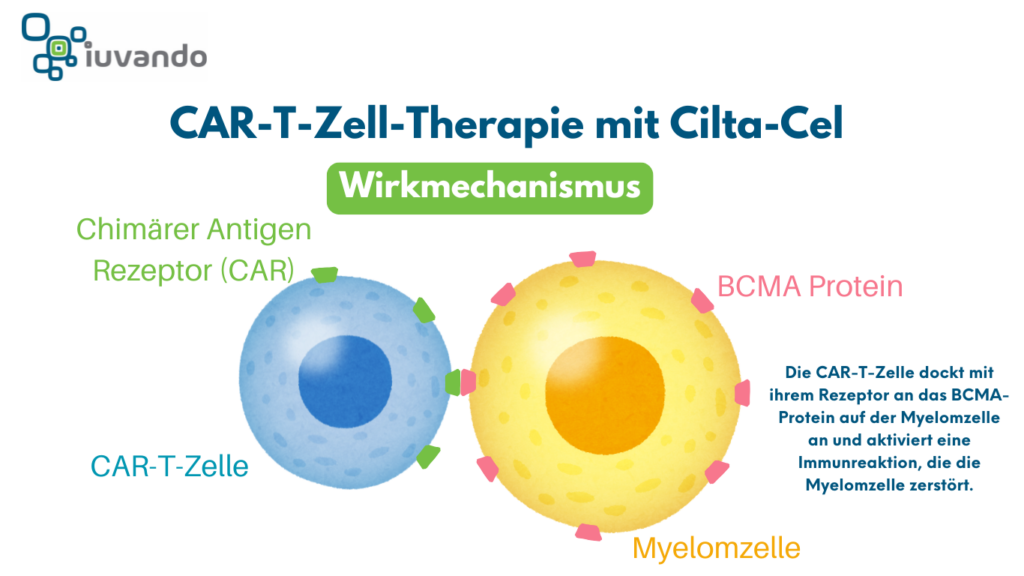
Abbildung: Wirkmechanimus der CAR-T-Zell-Therapie beim Multiplen Myelom am Beispiel von Cilta-Cel
Cilta-Cel ist ein speziell entwickeltes CAR-T-Zell-Produkt für PatientInnen mit Multiplem Myelom, bei denen herkömmliche Therapien nicht mehr wirken. Es richtet sich an PatientInnen mit mindestens einer früheren Behandlung, deren Krankheit jedoch weiter voranschreitet. Wichtig: Die Therapie darf nur in spezialisierten Kliniken durchgeführt werden.
Für wen kommt die CAR-T-Zell-Therapie infrage?
Aktuell ist die CAR-T-Zelltherapie für PatientInnen mit Multiplem Myelom zugelassen, bei denen die Erkrankung nach einer Therapielinie wieder aufgetreten ist oder die auf die Therapie nicht angesprochen haben. Die PatientInnen müssen zuvor mindestens mit einem Immunmodulator (z.B. Lenalidomid) und einem Proteasom-Inhibitor behandelt worden sein und gegen Lenalidomid refraktär sein. Sie wird insbesondere bei PatientInnen angewendet, die gegen Proteasom-Inhibitoren, Immunmodulatoren und Anti-CD38-Antikörper refraktär sind.
Welche CAR-T-Zell-Produkte sind für das Multiple Myelom zugelassen?
Derzeit sind zwei BCMA-gerichtete CAR-T-Zell-Produkte zugelassen:
- Idecabtagene Vicleucel (Abecma®)
- Ciltacabtagene Autoleucel (Carvykti®)
Beide zeigen hohe Ansprechraten, auch bei PatientInnen, die auf vorherige Therapien nicht mehr angesprochen haben.
Wie läuft die Behandlung mit CAR-T-Zellen ab?
Die Therapie erfolgt in mehreren Schritten:
- Leukapherese – Entnahme der T-Zellen aus dem Blut.
- Gentechnische Modifikation – Anpassung der T-Zellen im Labor, sodass sie Myelomzellen gezielt erkennen können.
- Lymphozytendepletion – Eine kurze Chemotherapie, um Platz für die veränderten T-Zellen zu schaffen.
- CAR-T-Zell-Infusion – Die gentechnisch modifizierten T-Zellen werden in den Körper zurückgegeben.
- Überwachung & Nachsorge – Engmaschige Kontrolle auf Nebenwirkungen und langfristige Effekte.
Hinweis: Die Therapie darf nur in spezialisierten Kliniken durchgeführt werden.
Was sind die häufigste Nebenwirkungen einer CAR-T-Zell Therapie?
CAR-T-Zell-Therapien können intensive Nebenwirkungen haben, zu den häufigsten gehören:
- Das Zytokinfreisetzungssyndrom (CRS) tritt bei rund 80 % der Patientinnen und Patienten auf: Es kommt zu einer Immunreaktion mit Fieber, Blutdruckabfall und Entzündungsreaktionen.
- Neurotoxizität (ICANS): Vorübergehende neurologische Probleme wie Verwirrtheit oder Sprachstörungen.
- Infektionsanfälligkeit: Durch die intensive Immunreaktion kann es zu erhöhter Infektanfälligkeit kommen.
Diese Nebenwirkungen treten meist in den ersten Wochen auf und erfordern eine Behandlung in einem spezialisierten Zentrum. Daher die Nebenwirkungen in wenigen Fällen auch mit zeitlicher Verzögerung auftreten können, muss die Nachsorge nach einer Behandlung mit CAR-T-Zellen an einem spezialisierten Zentrum erfolgen.
Übersicht zur Häufigkeit von CRS (Zytokinfreisetzungssyndrom) und ICANS (neurotoxische Nebenwirkungen) bei den beiden CAR-T-Zell-Therapien Idecabtagen Vicleucel (Abecma) und Ciltacabtagen Autoleucel (Cilta-Cel), basierend auf den Zulassungsstudien:
| Nebenwirkung | Abecma (KarMMa-Studie) | Cilta-Cel (CARTITUDE-1-Studie) |
|---|---|---|
| CRS (alle Schweregrade) | 84% | 95% |
| CRS (Grad 3 oder höher) | 9% | 5% |
| ICANS (alle Schweregrade) | 18% | 21% |
| ICANS (Grad 3 oder höher) | 3% | 9% |
Anmerkungen:
-
CRS ist bei beiden CAR-T-Zelltherapien häufig, aber meist mild bis moderat und gut behandelbar.
Wie wirksam ist die CAR-T-Zell-Therapie beim Multiplen Myelom?
Studien zeigen, dass mehr als 70–90 % der PatientInnen auf die Therapie ansprechen und die meisten für längere Zeit krankheitsfrei bleiben. Einige PatientInnen haben auch nach mehreren Jahren keine Krankheitsrückkehr.
Wirksamkeit von Cilta-Cel (Ciltacabtagene Autoleucel) aus der CARTITUDE-4-Studie und Abecma (Idecabtagene Vicleucel) aus der KarMMA-3-Studie:
| Parameter | Cilta-Cel (CARTITUDE-4) | Abecma (KarMMA-3) |
|---|---|---|
| Patientengruppe | Lenalidomid-refraktäres Multiples Myelom, 1–3 Vortherapien | Triple-Class-exponiertes Multiples Myelom, 2–4 Vortherapien |
|
Zeit ohne Krankheitsfortschritt oder Krankheitsrückfall (Progressionsfreies Überleben, PFS) |
Nicht erreicht (12-Monats-PFS: 75,9%) HR vs. Standard: 0,26 |
13,3 Monate (vs. 4,4 Monate mit Standardtherapie) HR vs. Standard: 0,49 |
| Gesamtansprechrate (ORR) | 84,6% | 71% |
| Komplette Remissionsrate (CR oder besser) | 73,1% | 39% |
| MRD-Negativität | 60,6% | 20% |
| Gesamtüberleben (OS) | 30-Monats-OS: 76,4% HR vs. Standard: 0,55 |
Daten noch nicht ausgereift |
Fazit:
-
Cilta-Cel zeigt in der CARTITUDE-4-Studie eine überlegene PFS- und ORR-Rate sowie eine höhere CR- und MRD-Negativitätsrate im Vergleich zu Abecma.
-
Abecma in der KarMMA-3-Studie ist ebenfalls effektiv, zeigt jedoch ein kürzeres PFS und eine geringere Rate tiefer Remissionen.
-
Beide CAR-T-Zelltherapien stellen hochwirksame Optionen für das Multiple Myelom dar.
Wie lange hält die Wirkung der CAR-T-Zellen an?
Die Dauer des Therapieerfolgs ist individuell verschieden. In Studien zeigen viele PatientInnen ein anhaltendes Ansprechen über ein bis mehrere Jahre, aber ein erneutes Fortschreiten der Krankheit ist möglich.
Wie hoch ist die Überlebensrate nach einer CAR-T-Zelltherapie beim Multiplen Myelom?
Aktuelle Langzeitdaten aus der CARTITUDE-4-Studie zeigen, dass Ciltacabtagen Autoleucel (Cilta-Cel) das Gesamtüberleben (OS) und die Zeit ohne ein Fortschreiten der Erkrankung (Progressions-freies Überleben, PFS) im Vergleich zur Standardtherapie (SOC) deutlich verbessert.
- Gesamtüberleben nach 30 Monaten: 76,4 % der PatientInnen, die Cilta-Cel erhielten, waren nach 30 Monaten noch am Leben, verglichen mit 63,8 % in der Standardtherapie-Gruppe.
- Kein Fortschreiten des Multiplen Myeloms (PFS): 59,4 % der PatientInnen in der Cilta-Cel-Gruppe waren nach 30 Monaten hatten ein anhaltendes Therapieansprechen, verglichen mit nur 25,7 % in der Standardtherapie-Gruppe. Dies entspricht einer 71%igen Reduktion des Risikos für ein Fortschreiten der Erkrankung oder Tod.
- Therapieansprechen: Die Gesamtansprechrate (ORR) lag bei 84,6 %, mit einem kompletten Ansprechen (sCR) bei 69,2 % der PatientInnen. Die sCR-Rate stieg im Verlauf der Studie weiter an (von 58,2 % nach 15,9 Monaten auf 69,2 % nach 33,6 Monaten), was auf ein nachhaltiges, tiefes Ansprechen hindeutet.
Die Ergebnisse zeigen, dass Cilta-Cel die erste CAR-T-Zell-Therapie ist, die einen deutlichen Überlebensvorteil beim Multiplen Myelom nachweist. Besonders bemerkenswert ist, dass das mittlere Gesamtüberleben und die mittlere Zeit ohne ein Fortschreiten des Multiplen Myeloms in der Cilta-Cel-Gruppe noch nicht erreicht wurden, was darauf hindeutet, dass viele PatientInnen über einen langen Zeitraum ohne Krankheitsrückfall bleiben.
Gibt es eine Erhaltungstherapie nach der CAR-T-Zell-Therapie?
Nein, aktuell wird nach einer CAR-T-Zell-Therapie keine Erhaltungstherapie durchgeführt. Die Therapie soll langfristig wirken, ohne dass kontinuierlich Medikamente eingenommen werden müssen. Es gibt erste Studien zu CAR-T-Enhancern, dies sind speziell entwickelte Wirkstoffe, die die Wirksamkeit der CAR-T-Zell aufrechterhalten sollen. Diese sind aktuell aber noch in Erprobung nicht allgemein verfügbar.
Wo kann ich eine CAR-T-Zell-Therapie erhalten?
Die Therapie wird nur in spezialisierten Zentren durchgeführt, die über die notwendige Erfahrung mit Zelltherapien verfügen. Eine Liste der zugelassenen kann über Fachgesellschaften angefordert werden. Alternativ sollten Sie hierzu ihre behandelnde Ärztin oder ihren behandelden Arzt fragen.
Kann ich an einer klinischen Studie zur CAR-T-Zell-Therapie teilnehmen?
Ja, es gibt aktuell laufende Studien, die die CAR-T-Zelltherapie auch in früheren Krankheitsstadien testen oder neue Therapieansätze untersuchen, z. B.:
- CARTITUDE-6: Vergleich der CAR-T-Zelltherapie mit autologer Stammzelltransplantation für PatientInnen mit neu diagnostiziertem Multiplen Myelom. Link zur Studienvignette
- Quintessential-2: GPRC5D-gerichtete CAR-T-Zellen als neue Option für PatientInnen mit rezidiviertem oder refraktärem Multiplen Myelom. Link zur Studienvignette
- Carlota01: Neue BCMA-CAR-T-Zell-Therapie. Link zur Studienvignette
- Dual-Targeting CAR-T-Zell Therapie: Gegen BCMA und GPRC5D dual gerichtete CAR T-Zell Therapie mit BMS-986453. Link zur Studienvignette
Ein Gespräch mit ihren behandelnden ÄrztInnen oder Studienberatern kann helfen, passende Studien für Sie zu finden.
Was ist der Unterschied zwischen der CAR-T-Zelltherapie und einer Stammzelltransplantation?
Die CAR-T-Zelltherapie und die autologe Stammzelltransplantation (ASZT) sind beides intensive Behandlungsformen beim Multiplen Myelom, unterscheiden sich jedoch grundlegend in ihrer Wirkweise und Zielsetzung.
1. Wirkmechanismus:
-
CAR-T-Zelltherapie:
-
Dabei werden körpereigene T-Zellen gentechnisch verändert, um gezielt Myelomzellen anzugreifen.
-
Die veränderten T-Zellen („CAR-T-Zellen“) erkennen ein spezifisches Zielmolekül auf den Krebszellen (z. B. BCMA) und zerstören sie aktiv.
-
Es handelt sich um eine Patienten-individuelle Immuntherapie.
-
-
Autologe Stammzelltransplantation (ASZT):
-
Die autologe Stammzelltransplantation dient dazu, das Knochenmark zu regenerieren, nachdem Einsatz einer hochdosierten Chemotherapie.
-
Die Krebszellen werden primär durch die Hochdosis-Chemotherapie (z. B. mit Melphalan) abgetötet.
-
Die transplantierten Stammzellen helfen dabei, das normale Blutsystem wiederherzustellen.
-
2. Dauer und Ablauf:
| Merkmal | CAR-T-Zelltherapie | Stammzelltransplantation |
|---|---|---|
| Dauer der Therapie | Wochen bis Monate (inkl. Herstellung der Zellen) | 3–4 Wochen (inkl. Hochdosis-Chemotherapie) |
| Vorbehandlung | Lymphozytendepletion (Chemotherapie) | Hochdosis-Chemotherapie |
| Haupttherapie | Infusion der genetisch veränderten T-Zellen | Rückgabe der zuvor entnommenen Stammzellen |
| Regenerationszeit | In der Regel 2-3 Wochen | Ca. 2–3 Wochen |
| Langzeitwirkung | Potenziell langanhaltende Immunantwort | Kein direkter Einfluss auf das Immunsystem |
3. Wirksamkeit und Langzeitprognose:
-
CAR-T-Zelltherapie führt häufig zu tiefen und langanhaltenden Remissionen, auch bei Patienten mit bereits mehrfach vorbehandeltem Myelom.
-
Stammzelltransplantation ist eine etablierte Therapie in der Erstbehandlung.
4. Nebenwirkungen von CAR-T-Zell-Therapie und autologer Stammzelltransplantation:
| Nebenwirkung | CAR-T-Zelltherapie | Autologe Stammzelltransplantation |
|---|---|---|
| Zytokinfreisetzungssyndrom (CRS) | Häufig (50–90%), meist mild bis moderat | Nein |
| Neurotoxizität (ICANS) | Möglich (bis zu 20%) | Nein |
| Infektionen | Möglich | Erhöht durch niedrige Blutzellen |
| Müdigkeit & Schwäche | Möglich | Häufig |
| Knochenmarksuppression | Weniger stark als bei ASZT | Stark, durch Chemotherapie |
5. Für welche Patienten ist welche Therapie geeignet?
-
CAR-T-Zelltherapie:
-
Vor allem für Patienten mit rezidiviertem/refraktärem Myelom, die bereits Vortherapien erhalten haben.
-
Wird aktuell in klinischen Studien auch in früheren Krankheitsstadien untersucht. Siehe auch Studienvignette der CARTITUDE-6 Studie
-
-
Autologe Stammzelltransplantation:
-
Standardtherapie für jüngere, fitte Patienten beim neu diagnostizierten Multiplen Myelom
-
Zusammenfassung:
Die CAR-T-Zelltherapie ist eine gezielte Immuntherapie, die Krebszellen direkt attackiert, während die Stammzelltransplantation eine Unterstützung nach Hochdosis-Chemotherapie ist. Beide Verfahren haben ihren festen Platz in der Myelomtherapie – die Entscheidung hängt von Krankheitsstadium, Vortherapien und individueller Eignung ab.
Ist eine Heilung des Multiplen Myeloms durch die CAR-T-Zell-Therapie möglich?
Aktuell gilt das Multiple Myelom weiterhin als nicht heilbar, aber durch moderne Therapien wie die CAR-T-Zell-Therapie können sehr tiefe und langanhaltende Remissionen erreicht werden.
In Studien, wie CARTITUDE-4 (Cilta-Cel) und KarMMa-3 (Abecma), konnten viele PatientInnen über mehrere Jahre ohne Krankheitsrückfall leben. Besonders vielversprechend sind hohe Raten an MRD-Negativität (keine nachweisbaren Myelomzellen mit modernen Tests), was auf eine sehr starke Reduktion der Krebszellen hinweist.
Allerdings erleiden viele PatientInnen irgendwann ein Rezidiv, weshalb die Langzeitwirkung noch weiter untersucht wird. Wissenschaftler arbeiten daran, durch frühere Anwendung der CAR-T-Zelltherapie, verbesserte Kombinationstherapien und duale CAR-T-Zellen eine potenzielle Heilung in Zukunft zu ermöglichen.
Einige Patienten erreichen durch diese intensiven Behandlungsstrategien und das Erreichen einer anhaltenden MRD-Negativität eine sehr tiefe Remission. Experten diskutieren, ob dies langfristig einem funktionellen Heilungszustand gleichkommen könnte. Derzeit ist es jedoch nicht möglich, von einer vollständigen Heilung zu sprechen.
Die Phase 2 aMMbition Studie (Link zur Studienvignette) untersucht, ob eine Heilung 5 Jahre nach einer CAR-T-Zelltherapie mit Cilta-cel bei PatientInnen mit einem Standardrisiko Myleom möglich ist. Die Heilung ist definiert als als eine Kombination aus anhaltender (mindestens 2 Jahre bestehender) Negativität der minimalen Resterkrankung (MRD) mit vollständigem Ansprechen und keine Anzeichen des Multiplen Myeloms in der Positronen-Emissions-Tomographie/Computertomographie (PET/CT) nach 5 Jahren.
Die passende Studie zu Ihrer Krebserkrankung
Möchten Sie wissen, ob eine klinische Studie für Ihre individuelle Situation in Frage kommt? Schreiben Sie uns über das Kontaktformular. Wir finden die passende Studie für Sie – kostenlos und unabhängig.
Informieren Sie sich bereits jetzt über aktuelle Therapie-Studien beim Multiplen Myelom
Über den iuvando Patientenblog
Wir brennen für Wissenschaft und wollen Ihnen komplizierte Themen rund um die Krebsforschung einfach verständlich machen, die neuesten Informationen zu Behandlungsmöglichkeiten teilen und mit Ihnen nützliche Tipps für das Leben mit Krebs austauschen.
Wir freuen uns, wenn Sie uns hier oder auf unseren Social Media Kanälen Facebook und instagram begleiten.
Quellen:
Mateos M-V, San-Miguel J, Dhakal, et al. Overall survival (OS) with ciltacabtagene autoleucel (cilta-cel) versus standard of care (SoC) in lenalidomide (len)-refractory multiple myeloma (MM): phase 3 CARTITUDE-4 study update. Presented at: 2024 International Myeloma Society Annual Meeting; September 25-28, 2024; Rio de Janeiro, Brazil. Abstract OA – 65.
Rakhshandehroo, T., Mantri, S.R., Moravej, H. et al. A CAR enhancer increases the activity and persistence of CAR T cells. Nat Biotechnol (2024). https://doi.org/10.1038/s41587-024-02339-4 Link zum Artikel
San-Miguel J et al. Cilta-cel or Standard Care in Lenalidomide-Refractory Multiple Myeloma. New England Journal of Medicine, Veröffentlichung am 5. Juni 2023, N Engl J Med 2023;389:335-347. Link zum Originalartikel
Berdeja, Jesus G et al. Ciltacabtagene autoleucel, a B-cell maturation antigen-directed chimeric antigen receptor T-cell therapy in patients with relapsed or refractory multiple myeloma (CARTITUDE-1): a phase 1b/2 open-label study The Lancet, Volume 398, Issue 10297, 314 – 324. Link zum Originalartikel
Lin, Yi et al. Consensus guidelines and recommendations for the management and response assessment of chimeric antigen receptor T-cell therapy in clinical practice for relapsed and refractory multiple myeloma: a report from the International Myeloma Working Group Immunotherapy Committee The Lancet Oncology, Volume 25, Issue 8, e374 – e387. Link zum Originalartikel
Kortüm, Martin et al. Onkopedia Leitlinien Multiples Myelom, Oktober 2024. Link zu Onkopedia