Therapiestudien
Wissen & Ressourcen
Über iuvando
Therapiestudien
Wissen & Ressourcen
Über iuvando

Brustkrebs (auch Mammakarzinom) ist eine bösartige Entartung der Drüsenzellen der Brust (lat.: Mamma). Er kann bei Frauen, aber auch bei Männern auftreten. Es kommt dabei zu einer unkontrollierten Zellteilung und Wucherung der entarteten Zellen, die in benachbartes Gewebe einwachsen können oder auch Absiedelungen (Metastasen) in entfernten Körperregionen bilden können.
Brustkrebs ist mit rund einem Drittel die häufigste Krebserkrankung bei Frauen. Das mittlere Erkrankungsalter liegt bei 64 Jahren. Jede achte Frau wird in ihrem Leben einmal an Brustkrebs erkranken – in Deutschland werden im Jahr durchschnittlich 50.000 neue Fälle festgestellt.
Bei Männern ist Brustkrebs hingegen sehr selten und Männer erkranken im Schnitt erst mit 71 Jahren.
Brustkrebs ist die häufigste Krebsart bei Frauen – auch bei Männern kann Brustkrebs auftreten.
Frauen ab dem 30. Lebensjahr wird dazu geraten, die gesetzliche Vorsorge einer jährlichen Tastuntersuchung der Brust beim Gynäkologen in Anspruch zu nehmen. Auch vor dem Erreichen des 30. Lebensjahres und natürlich darüber hinaus wird allgemein empfohlen, selbstständig einmal monatlich die Brust abzutasten und auf Veränderungen (z.B. Einziehungen, Rötungen, Schwellungen) zu achten. Ab dem 50. Lebensjahr erhalten Frauen alle 2 Jahre eine Einladung zur Mammographie – bis zur Vollendung des 70. Lebensjahres. Hierbei wird die Brust mit Röntgenstrahlen durchscannt, um auch kleinere Tumoren, die noch nicht tastbar sind zu erkennen. Zudem werden dabei auch Mikrokalkablagerungen sichtbar, die einen Hinweis auf eine Brustkrebserkrankung liefern können.
Jede Frau sollte ihre Brust einmal monatlich untersuchen – denn 80% aller Tumoren werden eigenständig durch die Patientin aufgedeckt und ein frühes Erkennen der Erkrankung führt zu einer besseren Heilungschance. Empfohlen wird, sofern ein regelmäßiger Zyklus besteht, eine Woche nach der letzten Regel die Selbstuntersuchung durchzuführen, da das Gewebe dann abgeschwollen und wenig verhärtet ist. Besteht keine Menstruation (z.B. nach der Menopause oder durch orale Kontrazeptiva), so kann die Selbstuntersuchung an einem festen Tag des Monats, beispielsweise immer am Ersten erfolgen.
Die Selbstuntersuchung beginnt mit einem Blick in den Spiegel: es wird auf Auffälligkeiten oder Unterschiede der beiden Mammae geachtet, die Beweglichkeit wird geprüft, indem abwechselnd der linke und der rechte Arm über den Kopf gehoben und wieder gesenkt werden. Sind keine Einziehungen, Rötungen, Schwellungen oder Einschränkungen in der Beweglichkeit zu sehen, so kann das Abtasten beginnen. Es sollte der gesamte Bereich, Quadrant für Quadrant der Brust, bis hin zur Achselhöhle untersucht werden. Die Seiten der Brust und der Bereich der Achselhöhle lassen sich hierbei mit gehobenem Arm derselben Seite besser tasten. Auch die Brustwarzen sollten getastet werden und es sollte darauf geachtet werden, ob Sekret austritt. Eine zweite Abtastung im Liegen kann empfehlenswert sein, da sich durch die Veränderung der Position manche Stellen besser untersuchen lassen. Generell muss leichter Druck ausgeübt werden, um das Drüsengewebe in der Tiefe spüren zu können. Vor allem junge Frauen mit dichtem Drüsengewebe müssen sich erst an die knotige Grundstruktur gewöhnen. Je öfter die Selbstuntersuchung durchgeführt wird, desto besser können Abweichungen erkannt werden.
Brustkrebs ist eine Diagnose die von einem Pathologen, d.h. Facharzt eines pathologischen Instituts, anhand der mikroskopischen Untersuchung einer Gewebeprobe (Biopsie) aus Tumorgewebe gestellt wird. Dabei unterscheidet sich das Aussehen der Krebszellen je nach Art des Tumors. Darüberhinaus können bestimmte „Färbungen“ mit Immun-Markern vom Pathologen angefertigt werden („Immunhistologie“). Dies kann ermöglichen, bestimmte Proteine (Eiweißstoffe) zu erkennen, die auf der Oberfläche von Krebszellen vorkommen und für eine bestimmte Tumorart charakteristisch sind. Auf diesem Wege kann die Diagnosestellung gesichert werden.
Für die Diagnosestellung ist in der Onkologie grundsätzlich ein histologischer oder immunhistologischer Befund des Pathologen eine Voraussetzung. Dafür muss Tumorgewebe gewonnen werden (Biopsie) – am häufigsten wird hierfür unter lokaler Betäubung in den Tumor „gestanzt“ (Stanzbiospie). Außerdem ist in selteneren Fällen eine Vakuumbiospie eine Möglichkeit der Probegewinnung.
Ohne feingewebliche Untersuchung einer Gewebeprobe (Histologie) oder zytologische Untersuchung von Tumorzellen (Zytologie) kann keine Krebsdiagnose gestellt werden. Hiefür ist immer eine Probenentnahme (Biopsie) notwendig.
Eine Diagnosestellung anhand von bildgebenden Verfahren (Ultraschall, Mammographie) ist nicht möglich. Diese Verfahren können eine Verdachtsdiagnose begründen und aufzeigen auf welchem Wege bzw. an welcher Stelle eine Gewebeprobe am günstigsten gewonnen werden kann. Die BIRADS Klassifikation ist ein Beispiel, mit dem im Ultraschall oder der Mammographie Befunde nach ihrer Wahrscheinlichkeit für das Vorliegen einer bösartigen Erkrankung eingeteilt werden können. Weiterhin ist die Bildgebung ganz entscheidend, wenn es um die Ausdehnungsdiagnostik geht, d.h. um die Frage wie groß ist der Tumor und welche Organe hat er befallen.
Mit der BIRADS Klassifikation können radiologische Befunde auf ihre Wahrscheinlichkeit, gutartig oder bösartig zu sein hin, beurteilt werden.
Ein Brustkrebs besteht aus entarteten Zellen, die sich vermehren und eine Geschwulst („Tumor“) bilden. Beim Brustkrebs sind dies Drüsenzellen der Brust, welche das Brustgewebe zu großem Teil ausfüllen. Es gibt feingeweblich betrachtet zwei Hauptarten: invasiv duktales Mammakarzinom (ausgehend von den Zellen der Drüsengänge) und invasiv lobuläres Mammakarzinom (ausgehend von den Zellen der Drüsenläppchen). Seltener kommen das tubuläre, das muzinöse oder das medulläre Mammakarzinom vor.
Einen Sonderfall stellt das inflammatorische Mammakarzinom dar, bei dem eine deutliche Entzündungsreaktion die Erkrankung begleitet.
Vorstufen, sogenannte Präkanzerosen, die noch keine Brustkrebserkrankung darstellen, sind das duktale Carcinoma in situ (DCIS) und die atypische duktale Hyperplasie (ADH).
Für die Behandlung ist vor allem die Unterteilung anhand der Oberflächenproteine entscheidend, die in der Immunhistologie (s.o.) bestimmt werden können.
Man untersucht die Zellen hierbei auf Östrogen- und Progesteronrezeptoren (Hormonrezeptoren für die weiblichen Wachstumshormone Östrogen und Progesteron) sowie auf HER2neu Rezeptoren (Rezeptoren für Wachstumsfaktoren).
Hormonrezeptor-positive Karzinome weisen auf ihren Oberflächen Rezeptoren für die weiblichen Wachstumshormone Östrogen und Progesteron auf und werden daher von diesen in ihrem Wachstum gefördert. Etwa 70% aller Mammakarzinome sind Hormonrezeptor-positiv.
Das Hormonrezeptor-positive Karzinom ist das häufigste Mammakarzinom.
HER2neu-positive Karzinome weisen auf ihren Oberflächen Rezeptoren für bestimmte Wachstumsfaktoren auf werden daher von diesen in ihrem Wachstum gefördert. Etwa 20% aller Mammakarzinome sind HER2neu-positiv.
Ein Triple Negatives Karzinom weist weder die beiden Hormonrezeptoren, noch den HER2neu Rezeptor auf seiner Oberfläche auf und wird daher als dreifach negativ bezeichnet. Etwa 15-20% aller Mammakarzinome sind Triple Negativ.
Ein Mammakarzinom kann sowohl Hormonrezeptor-positiv als auch HER2neu-positiv sein.
Neben der histologischen (feingeweblichen) bzw. immunhistologischen Einordnung des Tumorgewebes spielt die molekulargenetische Untersuchung eine Rolle, da das Erbgut des Tumors (DNA) bei einzelnen Patienten ganz individuelle Veränderungen (Mutationen) aufweisen kann. Diese können für die weitere Behandlung eine entscheidende Rolle spielen. Sie können durch Sequenzierung der Erbsubstanz aus Tumorgewebe bestimmt werden. Dies ist meist auch noch nachträglich anhand einer asservierten Probe möglich.
Bei jungen PatientInnen und familiärer Vorbelastung ist hierbei vor allem die Untersuchung auf Defekte in den Reparaturgenen des Erbguts wichtig – die BRCA1 und BRCA2 Gene sind die wichtigsten Vertreter dieser Art. Liegt eine Mutation vor, ist dies sowohl für die Therapie als auch für die Nachkommen der Betroffenen entscheidend, da dann eine erbliche Form von Brustkrebs vorliegt.
Bei der Therapieentscheidung, die der Patient zusammen mit seinen Ärzten trifft, spielen grundsätzlich krebsbezogene Faktoren sowie patientenbezogene Faktoren (Alter, Allgemeinzustand, Krankengeschichte etc.) eine Rolle.
Die krebsbezogenen Faktoren umfassen:
Das Grading beschreibt wie sehr sich die Tumorzellen von normalen Brustdrüsenzellen unterscheiden.
Die Wahl des Behandlungsverfahrens richtet sich vor allem nach dem Stadium der Erkrankung.
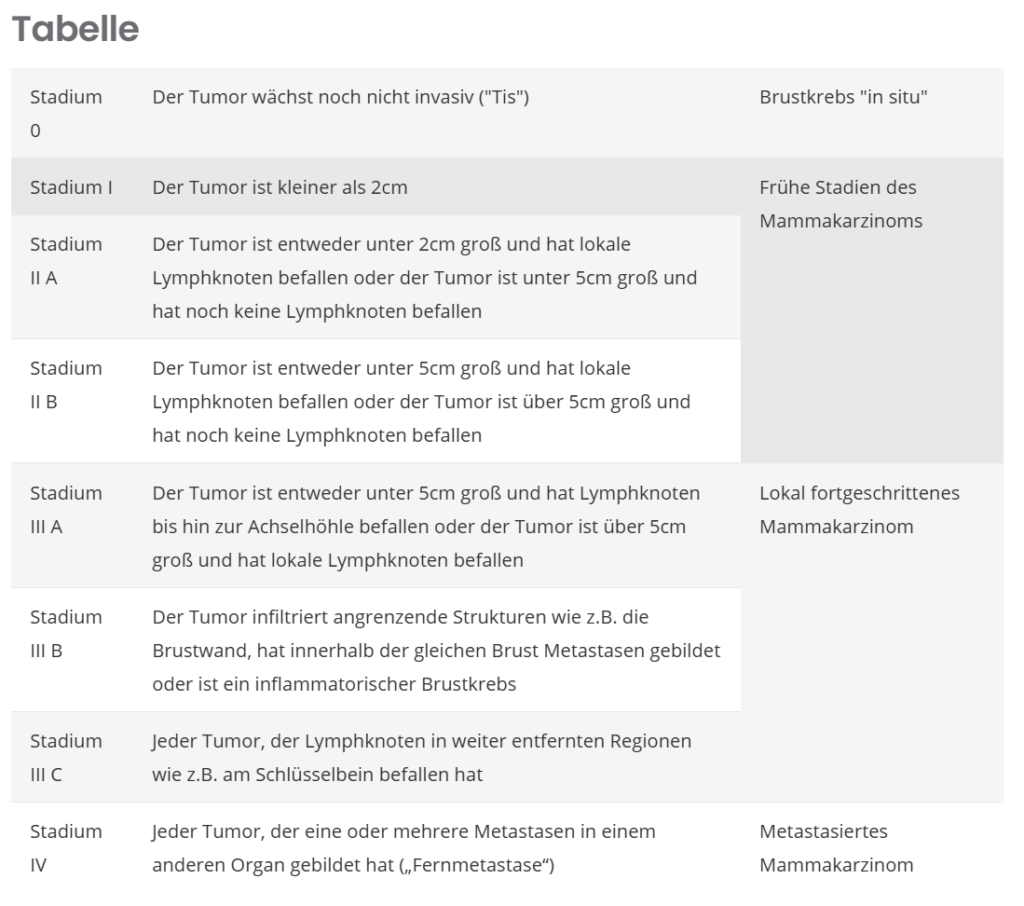
Beim Mammakarzinom haben sich die internationalen Fachgesellschaften auf folgendes Schema festgelegt (vereinfachte Darstellung):
Dies ist eine vereinfachte Darstellung. Beim Vorliegen bestimmter Kriterien, z.B. wenn der Tumor in benachbarte Strukturen wie die Brustwand eingewachsen ist oder ein entzündlicher Tumor (inflammatorischer Brustkrebs) vorliegt kann dies zur Einordnung der Erkrankung in ein höheres Stadium führen.
| Stadium 0 | Der Tumor wächst noch nicht invasiv („Tis“) | Brustkrebs „in situ“ |
| Stadium I | Der Tumor ist kleiner als 2cm | Frühe Stadien des Mammakarzinoms |
| Stadium II A | Der Tumor ist entweder unter 2cm groß und hat lokale Lymphknoten befallen oder der Tumor ist unter 5cm groß und hat noch keine Lymphknoten befallen | |
| Stadium II B | Der Tumor ist entweder unter 5cm groß und hat lokale Lymphknoten befallen oder der Tumor ist über 5cm groß und hat noch keine Lymphknoten befallen | |
| Stadium III A | Der Tumor ist entweder unter 5cm groß und hat Lymphknoten bis hin zur Achselhöhle befallen oder der Tumor ist über 5cm groß und hat lokale Lymphknoten befallen | Lokal fortgeschrittenes Mammakarzinom |
| Stadium III B | Der Tumor infiltriert angrenzende Strukturen wie z.B. die Brustwand, hat innerhalb der gleichen Brust Metastasen gebildet oder ist ein inflammatorischer Brustkrebs | |
| Stadium III C | Jeder Tumor, der Lymphknoten in weiter entfernten Regionen wie z.B. am Schlüsselbein befallen hat | |
| Stadium IV | Jeder Tumor, der eine oder mehrere Metastasen in einem anderen Organ gebildet hat („Fernmetastase“) | Metastasiertes Mammakarzinom |
Die Stadieneinteilung der Krebserkrankung erfolgt zunächst anhand klinischer bildgebender Verfahren, d.h. die Tumorgröße wird z.B. in den CT-Bildern ausgemessen und der Lymphknotenbefall anhand der Bilder beurteilt. In diesem Fall geht dem T oder N ein „c“ voraus.
Wenn ein Tumor operativ entfernt wird, kann der er in der Begutachtung durch den Pathologen genau vermessen werden. Auch die Lymphknoten können mikroskopisch auf Tumorbefall untersucht werden. Dies ist dann durch ein „p“ gekennzeichnet. Wenn in der Tumorformel zusätzlich ein „y“ auftaucht, bedeutet dies, dass die Beurteilung nach neoadjuvanter (d.h. vor Operation) Chemotherapie erfolgt ist, ein „r“ steht für „Rezidiv“, d.h. für einen wieder aufgetretenen Tumor.
Zu den Behandlungsmodalitäten zählen Operation, Strahlentherapie, Chemotherapie und zielgerichtete Krebstherapien, zu denen man sowohl die Antihormon- als auch die Anti-HER2-Therapie zählen kann.
Bei Diagnose eines Mammakarzinoms in einem frühen Stadium ist die Heilung des Patienten das Ziel. Man spricht von kurativer Behandlung.
Eine palliative Behandlung hat nicht die Heilung zum Ziel, sondern eine möglichst lange Erhaltung der Lebensqualität.
Die operative Entfernung des Tumors kommt in Frage, wenn ein Mammakarzinom im Frühstadium diagnostiziert wird. Dabei hängt die Auswahl des Operationsverfahrens von Größe und Lage des Tumors ab. Man unterscheidet im Einzelnen:
Eine Nebenwirkung nach der operativen Entfernung von Brustgewebe und anliegenden Lymphknoten kann die Entstehung eines Lymphödems sein – hierfür kommen dann weitere anschließende Behandlungen mit Lymphdrainage oder Kompression in Frage.
Eine Operation ist die bevorzugte Standardtherapie bei Brustkrebs im nicht-metastasierten Stadium (Stadium I, II und III). Dabei ist das Ziel der Behandlung die Heilung des Patienten. Bei der Operation werden der Tumor selbst sowie einige der benachbarten Lymphknoten im operativ entfernt. Da es sich bei der Entfernung des Tumors um einen operativen Eingriff handelt, wird bei der Therapieplanung das Alter des Patienten, der Allgemeinzustand und die medizinische Vorgeschichte (Begleiterkrankungen) genau geprüft. Ob ein Tumor entfernt werden kann, hängt nicht nur von seiner Größe und Lage ab, sondern auch von der Frage, ob ein Patient den Eingriff voraussichtlich gut verkraften kann. Im Vergleich zu anderen Krebserkrankungen ist die Operation bei Brustkrebs in den meisten Fällen ein relativ unkomplizierter operativer Eingriff, insbesondere, wenn die Brust erhalten werden kann.
In einem frühen Stadium kann das Mammakarzinom sehr häufig durch eine Operation geheilt werden.
Die Lymphknoten, die bei Brustkrebs befallen sein können, liegen zunächst im Brustdrüsengewebe selbst bis hin zur Achselhöhle oder zur Brustwand. In fortgeschritteneren Stadien können auch entferntere Lymphknoten z.B. über dem Schlüsselbein oder am Hals betroffen sein.
Die Frage, ob benachbarte Lymphknoten von Tumorzellen befallen sind, hat beim Mammakarzinom wie bei allen Tumoren eine wichtige Bedeutung für die Prognose des weiteren Verlaufs. Der Befall von Lymphknoten spielt daher bei der Stadieneinteilung mit Hilfe der TNM-Klassifikation eine entscheidende Rolle. Wenn Lymphknoten befallen sind, ist von einem höheren Risiko auszugehen, dass es nach operativer Entfernung zu einem Wiederauftreten (Rezidiv) des Tumors kommt. In der Operation wird daher nicht nur der Tumor, sondern auch angrenzende Lymphknoten entfernt. Die Zahl der entfernten Lymphknoten hängt dabei vom Operationsverfahren ab, das zur Anwendung kommt. Die während der Operation entfernten Lymphknoten werden unter dem Mikroskop auf das Vorhandensein von Krebszellen untersucht, so dass bereits während der Operation das Vorgehen angepasst werden kann.
Eine besondere Rolle spielen beim Brustkrebs die sogenannten Wächterlymphknoten (Sentinel Lymph Nodes). Vor der Operation wird eine farbige Flüssigkeit in die Lymphabflusswege der betroffenen Brust eingespritzt, die die Lymphknoten markiert, die am Übergang zur Achselhöhle stehen und den Abfluss „überwachen“ – dort reichert sich die Flüssigkeit an. Sind ein oder mehrere dieser Wächterlymphknoten vom Krebs betroffen, wird das Operationsverfahren dementsprechend angepasst, dass weitere Lymphknoten aus der Achselhöhle mitentfernt werden.
Je nach Tumorgröße und-beschaffenheit und je nachdem, ob und wie viele Lymphknoten befallen sind, kann vor der Operation eine zusätzliche („neoadjuvante“) Chemotherapie oder empfohlen werden. Vorzugsweise besteht die neoadjuvante Chemotherapie aus einer Kombination aus 4 Zyklen Epirubicin und Cyclophosphamid und der zwölfmaligen, wöchentlichen Gabe von einem weiteren Arzneimittel, Paclitaxel.
Wenn der Tumor HER2 neu positiv ist, kann auch eine zielgerichtete neoadjuvante Therapie mit einem Antikörper, der gegen den HER2 neu Rezeptor gerichtet ist, erfolgen (z.B. Trastuzumab und/oder Pertuzumab). Diese wird meistens in Kombination mit dem Chemotherapeutikum Docetaxel verabreicht.
Auch, wenn ein Tumor in der Operation vollständig entfernt werden kann, wird häufig eine adjuvante Strahlentherapie empfohlen, um die Wahrscheinlichkeit eines Wiederauftretens des Tumors zu senken. Insbesondere dann, wenn mehrere Lymphknoten befallen sind und auch die Achsellymphknoten mit entfernt werden mussten. Die adjuvante Strahlentherapie erfolgt in der Regel etwa 4-6 Wochen nach der Operation.
Bei einem Hormonrezeptor positiven Mammakarzinom wird im Anschluss an die Operation und gegebenenfalls die Strahlentherapie eine adjuvante endokrine Therapie durchgeführt. Hierbei werden in der Regel für 5-10 Jahre Tabletten eingenommen, die die weiblichen Hormone im Körper unterdrücken, sodass die Wahrscheinlichkeit für ein Wiederauftreten des Tumors vermindert wird.
Bei einem HER2 neu positiven Mammakarzinom wird eine adjuvante Therapie mit zielgerichteten Antikörpern gegen die HER2 neu Rezeptoren durchgeführt (z.B. Trastuzumab und/oder Pertuzumab). Hierbei handelt es sich um Infusionen oder Spritzen in das Unterhautfettgewebe, die über ein Jahr lang wöchentlich oder auch im 3 Wochen Takt appliziert werden.
Zusätzlich kann in beiden Fällen sowie auch beim Triple Negativen Mammakarzinom eine adjuvante Chemotherapie empfohlen werden, je nachdem wie groß der Tumor war, welche Beschaffenheit er hatte und wie viele Lymphknoten befallen waren.
Grundsätzlich besteht im metastasierten Stadium eine palliative Situation. Das Ziel der Behandlung besteht darin, ein Wachstum des Tumors aufzuhalten und so die Lebensqualität zu verbessern und möglichst lange zu erhalten. Ein operatives Vorgehen spielt in diesem Stadium eine untergeordnete Rolle, da häufig mehrere Metastasen vorliegen und diese erst ab einer bestimmten Größe mit bildgebenden Verfahren (CT) nachweisbar sind. Häufig hat der Tumor bereits unerkannt in weitere Körperregionen gestreut.
An erster Stelle steht in diesem Stadium eine systemische Krebsbehandlung, d.h. eine Therapieform, die den gesamten Körper erreicht. Dazu zählen neben der intravenösen Chemotherapie auch zielgerichtete Therapien in Tablettenform (z.B. die endokrinen Antihormontherapien), als Infusion oder Spritze unter die Haut (z.B. HER2 neu-Antikörper) sowie neue Therapieformen wie sie in klinischen Studien angeboten werden (z.B. zelluläre Therapien / adoptive Immuntherapien). Welche Therapie empfohlen wird richtet sich vor allem nach dem histologischen und molekulargenetischen Typ des Tumors, d.h. dem Hormonrezeptor- und dem HER2neu Rezeptor-Status.
Möglicherweise werden Sie von Ihren Ärzten gefragt, ob Sie an einer klinischen Studie teilnehmen möchten. Dabei handelt es sich um wissenschaftliche Studien der Krebsforschung, die mit Patienten durchgeführt werden, um neue Behandlungsmöglichkeiten zu prüfen und die Wirksamkeit und Verträglichkeit neuer Wirkstoffe herauszufinden.
Klinische Studien tragen dazu bei, neue Erkenntnisse über Krebserkrankungen zu gewinnen, daher kann die Teilnahme an einer solchen Studie mit verschiedenen Vorteilen für Sie verbunden sein. Beispielsweise werden Sie während und nach einer Studienteilnahme besonders sorgfältig überwacht. Es kann sein, dass die neue Behandlung einen größeren Nutzen als herkömmliche Therapien für Sie erbringt. Es kann aber auch sein, dass sich manche der neuen Behandlungen als nicht so wirksam wie die herkömmlichen herausstellen oder Nebenwirkungen haben, die ihren Nutzen überwiegen.
Jedes Arzneimittel wurde vor der Zulassung über Jahre in klinischen Studien erprobt. Eine Teilnahme an einer klinischen Studie kann mit Vorteilen verbunden sein.
Sie haben das Recht, der Teilnahme an einer klinischen Studie zuzustimmen oder eine Teilnahme abzulehnen, ohne dass dadurch die Qualität Ihrer Versorgung beeinträchtigt wird. Es kann auch sein, dass Ihre Ärzte Ihnen nicht den Vorschlag machen, an einer klinischen Studie teilzunehmen. Wenn Sie dennoch mehr über diese Möglichkeit erfahren möchten, fragen Sie nach, ob es eine klinische Studie für Ihre Krebserkrankung in Ihrer Nähe gibt oder beauftragen Sie uns vorab mit der Erstellung einer personalisierten Studienübersicht, die Sie anschließend mit Ihren Ärzten besprechen können.
Finden Sie hier eine Übersicht der Therapiestudien, die aktuell an deutschen Kliniken Patienten mit Brustkrebs aufnehmen können (geordnet nach Rezeptorstatus und Therapielinie). Die Übersicht erhebt keinen Anspruch auf Vollständigkeit und beschränkt sich auf medikamentöse Phase 3-Studien. Sehr gerne schauen wir individuell für Sie welche Studien gemäß der Ein- und Ausschlusskriterien passend sind und in Ihrer Nähe angeboten werden.
Onkopedia Leitlinien, “Lungenkarzinom, kleinzellig (SCLC)”, Stand 2019
NCCN Guidelines for Patients®: “Small Cell Lung Cancer”, 2022
Clinicaltrials.gov “Learn about clinical studies”. Verfügbar unter https://clinicaltrials.gov/ct2/about-studies/learn. Abgerufen am 14.10.2022.
Stand: 14.11.2022, erstellt von: Cheyenne Collins, Dr. med. Benjamin Hanfstein
Kennen Sie alle Therapieoptionen für Ihre Krebserkrankung?
Individuelle Beratung durch unsere Experten
Lieber telefonieren?
Lassen Sie sich von uns beraten – kostenlos und unverbindlich
Weitere Artikel
There are no results matching your search
Erfahren Sie hier alle Behandlungsoptionen für Ihre individuelle Krebserkrankung
Wir unterstützen Krebspatienten dabei, passende klinische Studien zu finden – kostenlos, persönlich und mit Expertenwissen.
Wichtig: In den Texten auf unserer Webseite benutzen wir einheitlich die männliche Form. Das ist leichter zu lesen. Gemeint sind alle Menschen.
© 2026 iuvando GmbH. Alle Rechte vorbehalten.
Mit Hoffnung und Expertise für Patienten.